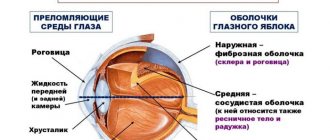
Причины возникновения
Дистрофия Беста по методу наследования отнесена к аутосомно-доминантному типу. К развитию заболевания прямое отношение имеет ген, который находится на длинном плече хромосомы номер одиннадцать.
Заранее выявить заболевание невозможно, оно проходит бессимптомно. В редких случаях пациенты могут жаловаться на проблемы с чтением мелкого шрифта, иногда наступающее затуманивание зрения, а также метаморфопсии. Особенно часто подобную патологию выявляют случайно на очередном офтальмологическом осмотре.
Патология, которая передается по наследству
Больше века назад Ф.Бест проанализировал идентичные нарушения зрения, которыми страдали несколько родственников, — представителей одной семьи. На основе проведенной работы он сделал вывод, что макулярная дистрофия такого типа имеет наследственную природу.
Сегодня ученым известно, что патологию ребенок наследует от своих родителей, при этом вероятность передачи дефектного гена сохраняется даже при условии, что его носителем является только мама или только папа (аутосомно-доминантный тип наследования).
Признаки заболевания
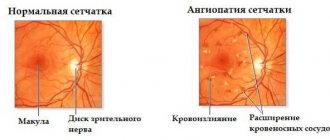
Дистрофия Беста возникает вследствие скопления транссудата под пигментным эпителием. Подобное скопление иногда может достигать трех размеров диаметра диска зрительного нерва и вести к офтальмологическим изменениям в зоне макулы глаза. В зависимости от интенсивности подобных изменений, принято выделять определенные стадии развития заболевания:
- Превителлифомную стадию, когда в макуле обнаруживаются мелкие желтые пятна и минимальное нарушение пигментации;
- Вителлиформную стадию с вителлиформной кистой в макуле;
- Стадию разрыва кисты и резорбции её содержимого;
- Стадию образования фиброглиального рубца.
В своем развитии, болезнь Беста строго проходит стадии не всегда, иногда возможны незначительные вариации проявлений заболевания. Изменения, как правило, имеют двусторонний, асимметричный характер. Острота зрения снижается только к 3-ей стадии, оставаясь в пределах от 0,02 до 1,0D. С течением времени возможна дегенерация внешних составляющих фоторецепторов. Без должного адекватного лечения болезнь Беста может быть осложнена образованием субретинальной мембраны и субретинальными кровоизлияниями. В редких случаях, подобное состояние может привести к отслойке сетчатки, а также хориоидальному склерозу.
Как патология влияет на зрительную функцию?
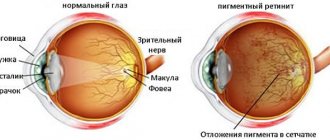
На раннем этапе болезнь часто протекает бессимптомно, не влияет на качество зрения и заметить ее можно только в том случае, если ребенок регулярно проходит плановые офтальмологические осмотры. Во время обследования врач может обнаружить на глазном дне специфические изменения, указывающие на начало развития болезни Беста.
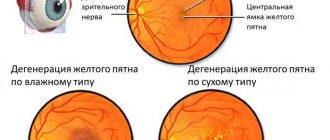
Первый внешний симптом, который может сигнализировать о развитии детской макулярной дегенерации, — это незначительное ухудшение зрительной остроты. Во время обследования на такой стадии можно увидеть в центре сетчатки желтые точки. Развитие болезни приводит к разрастанию этих точек и формированию кист. Если пациент жалуется на сильное снижение и затуманенность зрения, это может свидетельствовать о том, что произошел разрыв кист (характерный симптом третьей стадии заболевания).
Самые сильные нарушения характерны для четвертой стадии: зрение снижается очень сильно, в зрительном поле возникают скотомы — участки полной слепоты.
Диагностика болезни Беста
Диагностирование детской дегенерации желтого пятна происходит на основании результатов офтальмоскопии, показаний электроретинографии и электроокулографии. Нередко для ее подтверждения применяют и флуорисцентную ангиографию. В сложных ситуациях для помощи в диагностике может понадобиться обследование членов семьи пациента.
В случае четко выраженной желточной кисты поставить диагноз, труда не составляет, но при нечетких границах кисты и резорбции ее содержимого, необходимо провести дифференциальную диагностику. Дифференцировать болезнь Беста необходимо от миопического макулита, болезни Штаргардта, серозного отека макулы, кистозной дистрофии макулярной зоны, хороидита.
Болезнь Беста — симптомы и лечение
Для постановки диагноза «болезнь Беста» необходим ряд обследований. В первую очередь нужно зарегистрировать специфическую офтальмоскопическую картину глазного дна, характерную для каждой стадии заболевания. Затем, чтобы оценить состояние сетчатки, следует выполнить электроокулографию (ЭОГ) и электроретинографию (ЭРГ). В последние годы, с развитием генетики, стало обязательным молекулярное генетическое исследование пациента. Вместе с этим производят офтальмологическое и генетическое обследование других членов семьи.
Офтальмоскопия позволяет обнаружить первые признаки болезни Беста на первом и втором десятилетии жизни. На первых стадиях в макуле появляются желтоватые очажки, затем формируются виттелиформные кисты, при разрывах которых глазное дно напоминает картину «яичницы-глазуньи». На последних стадиях в макуле формируется атрофические глиальные рубцы, а при осложнениях — неоваскулярная мембрана и сквозные макулярные отверстия.
Электроокулография является очень важным методом диагностики при болезни Беста. С её помощью можно выявить такой специфический признак заболевания, как снижение коэффициента Ардена — соотношения биопотенциала глаз в темноте и при свете. Данный показатель будет снижен даже на нулевой стадии болезни при нормальной офтальмоскопической картине. В случае вителлиформной макулодистрофии взрослых электроокулография изменений не выявит.
Флюоресцентная ангиография позволяет диагностировать болезнь Беста даже на доклиническом этапе. Изменения сетчатки зависят от стадии заболевания. На начальном этапе болезни видны мелкие окончатые дефекты и участки с локальной гиперфлюоресценцией (свечением). При наличии сформированной кисты флюоресценция полностью отсутствует. На третьей стадии болезни гиперфлюоресценция наблюдается только в верхней части кисты, а в нижней её части отсутствует [8].
При электроретинографии (общей и ритмичной) наблюдается снижение амплитуды «а» волн, увеличение латентных периодов «а» и «b» волн, а также угнетение ответа от центральных отделов сетчатки [9].
Статическая компьютерная периметрия выявляет снижение чувствительности макулярной области, а при разорвавшейся вителлиформной кисте — центральную абсолютную скотому (слепое пятно). При этом границы поля зрения по периферии остаются в норме.
Дифференциальная диагностика
Болезнь Беста необходимо отличить от других заболеваний:
- болезни Коатса и других макулярных дистрофий пигментного эпителия сетчатки (Х-образной макулярной дистрофии);
- острого хориоретинита (в первую очередь токсоплазмозной этиологии);
- болезни Штаргардта;
- вителлиформной дистрофии взрослых;
- отслойки пигментного эпителия сетчатки [11].
Болезнь Коатса — врождённая ненаследственная патология, при котором наблюдаются аномалии сосудов сетчатки глаза. Она может стать причиной частичной или полной слепоты. На первых стадиях болезнь Коатса так же, как и болезнь Беста, течёт без симптомов и в большинстве случаев диагностируется у детей 2-8 лет при случайных профилактических осмотрах, проводимых в детских садах или школах. В отличие от болезни Беста, при болезни Коатса, как правило, в патологический процесс вовлекается только один глаз. Лишь у 5-8 % больных наблюдаются двусторонние изменения. Мальчики заболевают им в 3 раза чаще, чем девочки [9].
У большинства пациентов с заболеванием Коатса во время первого офтальмологического обследования в центральной области сетчатки выявляют возвышающийся округлый очаг твёрдого желтоватого экссудата, очень похожий на вителлиформные изменения, встречающиеся при болезни Беста. Данные экссудаты в центральной области сетчатки очень часто сочетаются с кровоизлияниями за сетчаткой и образованием новых сосудов, что тоже характерно для болезни Беста.
Диагностика болезни Коатса основывается на результатах осмотра глазного дна (офтальмоскопии), а также центральной области и периферии глазного дна с применением или налобного офтальмоскопа с линзами 20-30 дптр, или офтальмобиомикроскопии с трёхзеркальной линзой Гольдмана. У большинства пациентов с болезнью Коатса во время данного обследования обязательно выявляются аномалии сосудов: микро- и макроаневризмы, телеангиэктазии (сосудистые звёздочки), артериовенозные шунты. Чаще всего эти аномалии располагаются в височной половине сетчатки.
Изменения при электроокулографии в начальной и развитой стадиях заболевания, как и при болезни Беста, не выявляются. Но острота зрения у больных с ретинитом Коатса низкая: при наличии изменений в центральной области сетчатки она не превышает 0,4, а при болезни Беста длительно сохраняются в норме [7].
Острый токсоплазмозный хориоретинит — это паразитарное заболевание глаз, для которого характерно в основном скрытое или хроническое течение. Как правило, оно поражает только один глаз, в отличие от болезни Беста. При неадекватном и несвоевременном лечении может привести к стабильному снижению остроты зрения.
Трудности при диагностике обычно возникают при обследовании больных с приобретённым токсоплазмозом и экссудативно-геморрагическими изменениями в центральной области сетчатки, которые похожи на вителлиформные очажки с субретинальными геморрагиями, как при болезни Беста. Хориоретинальные поражения при токсоплазмозе сочетаются с выпотом в стекловидное тело различной степени тяжести, а порой и изменениями переднего отрезка глаза.
Пациенты, как правило, предъявляют жалобы на внезапное, резкое и значительное снижение центральной остроты зрения, которая в ряде случаев изменяется до 0,01-0,2. При статической периметрии регистрируется повышенный порог яркостной чувствительности, относительная или абсолютная центральная скотома. Электроокулография, как правило, не изменена.
Для подтверждения и верификации токсоплазмоза необходимо выполнить иммунологические исследования, определить антитела к токсоплазме или выделить её методом ПЦР (полимеразной цепной реакции). В 95 % случаев токсосплазмозный хориоретинит хорошо поддаётся лечению, острота зрения может восстановиться до исходных значений [12].
Болезнь Штаргардта иначе называют ювенильной макулярной дегенерацией. Впервые это заболевание описал немецкий врач-офтальмолог К. Штаргардт как врождённое поражение макулы, которое передавалось по наследству в одной семье.
Как правило, болезнь Штаргардта начинается в молодом (ювенильном) возрасте и сопровождается поражением центральной области сетчатки, как и болезнь Беста. Её отличает быстрое прогрессирование, вплоть до инвалидизации. Медленное ухудшение зрения встречается крайне редко (при доминантном типе наследования) [9].
Данное заболевание всегда двустороннее и симметричное. Его характерными признаками являются различные процессы: атрофия хориоидеи (сосудистой оболочки глаза), «бычий глаз», очаг дистрофии цвета «битой (кованой) бронзы» и др. При далеко зашедшем процессе фовеолярный рефлекс (центральная ямка макулы) отсутствует. В макулярной области на уровне пигментного эпителия сетчатки наблюдаются скопления коричневатого, тёмного пигмента, который окружён участками гипер- и депигментации. Эти скопления отличаются от вителлиформных жёлтых очагов при болезни Беста.
Вителлиформная макулодистрофия взрослых, в отличие от болезни Беста, развивается у людей 40-50 лет. Для неё характерно двустороннее симметричное поражение макулы с локальными изменениями. Очаги патологии, как правило, имеют округлую форму и жёлтый оттенок. Их отличает отсутствие прогрессирования и небольшие размеры: диаметр поражений достигает 0,3-0,5 размера диска зрительного нерва. При этом нарушения зрительных функций минимальны.
Вещества, подобные липофусцину, скапливаются диффузно в различных местах: в пигментном эпителии, внутренней части фоторецепторов, мюллеровских клетках и даже в стекловидном теле.
Отслойка пигментного эпителия сетчатки возникает при нарушении нормального соединения пигментного эпителия сетчатки с мембраной Бруха. К причинным факторам относятся сосудистые, воспалительные и дистрофические процессы.
Длительное время болезнь может существовать без какой-либо динамики, спонтанно исчезать, а вследствие инвазии сосудов из хориоидеи трансформироваться в геморрагическую отслойку. Сложности в диагностике могут возникнуть при атипичной клинической картине заболевания и экссудативных изменениях в центральной области сетчатки.
Обычно болезнь поражает только один глаз. Общая электроретинография не меняется, локальная — может быть снижена. Электроокулография, как правило, в норме. При флюоресцентной ангиографии на последней стадии отслойки регистрируется гиперфлюоресценция.
Лечение заболевания
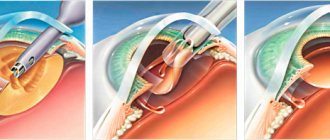
Действенного и эффективного лечения болезни Беста в настоящее время не существует. Так как, заболевание обычно бессимптомно, беспокоящих пациента, врачи, как правило, не предпринимают каких-либо особых мер. В случае формирования субретинальной мембраны, которая способна вызывать незначительные дефекты зрения, иногда проводится лазерная коагуляция сетчатки.
В сравнении с болезнью Беста, дегенерация желтого пятна у взрослых не прогрессирует, кроме того, она сопровождается меньшими очагами поражения.
В медицинском все желающие могут пройти обследование на самой современной диагностической аппаратуре, а по результатам – получить консультацию высококлассного специалиста. Мы открыты семь дней в неделю и работаем ежедневно с 9 ч до 21 ч. Наши специалисты помогут выявить причину снижения зрения, и проведут лечение выявленных патологий. Опытные рефракционные хирурги, детальная диагностика и обследование, а также большой профессиональный опыт наших специалистов обеспечивают благоприятный результат для пациента.
Узнать стоимость той или иной процедуры, записаться на прием в «Московскую Глазную Клинику» Вы можете по многоканальному телефону 8 (ежедневно с 9:00 до 21:00, бесплатно для мобильных и регионов РФ) или заполнив форму онлайн-записи.
Яковлева Юлия Валерьевна
Потеря зрения при болезни Беста неизбежна?
Несмотря на то что болезнь Беста сегодня не лечится (существует лишь поддерживающая терапия, замедляющая дистрофический и дегенеративный процессы), офтальмологи дают хороший прогноз по сохранению зрительной функции. Главное условие — ранняя диагностика, которая помогает вовремя начать лечение, замедлить патологический процесс и сохранить зрение. Вот почему так важно в детском возрасте посещать офтальмолога хотя бы раз в год. Если родители знают об отягощенной наследственности, то посещения врача должны быть более частыми.
Команда MagazinLinz.ru
Диагностика
Врач-пульмонолог проводит физикальный осмотр, аускультацию (выслушивание) и перкуссию (простукивание) органов дыхания. Диагноз асбестоз устанавливают на основании тщательно собранного анамнеза, выяснения обстоятельств и длительности воздействия асбеста, оценки функции внешнего дыхания (спирометрии), рентгенографии (или КТ) грудной клетки. Эти диагностические данные помогают врачу оценить работу легких и тяжесть течения заболевания.
В некоторых случаях, для уточнения диагноза, может потребоваться проведение дополнительных исследований:
- бронхоскопия — визуализация слизистых трахеи и бронхов (с биопсией — для последующего диагностического исследования жидкости или ткани легких);
- плевроцентез — плевральная пункция (для удаления жидкости между легкими и плевральной полостью и исследования полученного материала).
Обследование при дистрофии сетчатки
Для диагностики необходимо провести такие исследования:
Визометрия – острота зрения от нормальной (в начальной стадии) до полной слепоты. Коррекции не поддается; — периметрия – сужение поля зрения, от появления скотом до трубчатого зрения; — тест Амслера – простейший субъективный способ диагностики макулодистрофии. Пациента просят закрыть один глаз и смотреть на точку в центре сетки Амслера на расстоянии вытянутой руки, затем медленно приближают тест, не отрывая взгляд от центра. В норме линии не искажаются
Тест амслера: 1. норма 2. Патология
Рефрактометрия – для диагностики аномалий рефракции (дегенерация сетчатки возможна при высокой миопии); — биомикроскопия позволяет выявить сопутствующую патологию; — офтальмоскопия проводится после медикаментозного расширения зрачка, желательно с линзой Гольдмана для более детального осмотра сетчатки, в частности периферии. При различных видах дистрофий врач видит разную картину глазного дна; — определение цветового зрения – таблицы Рабкина и др.; — электроретинография – показатели снижены или не регистрируется при большинстве наследственных дистрофий; — адаптометрия – исследование темновой адаптации — снижение или отсутствие темнового зрения при поражении колбочек; — флуоресцентная ангиография для определения участков, где необходимо провести лазерную коагуляцию сетчатки; — оптическая когерентная томография сетчатки
HRT (Хайдельбергская ретинотомография); — УЗИ глаза; — общеклинические анализы; — консультация терапевта, педиатра, генетика и других специалистов по показаниям.
Лечение дистрофии сетчатки
В зависимости от клинической картины и вида дистрофии назначают лечение. Практически всегда лечение симптоматическое, так как все дегенерации, кроме вторичных, имеют наследственный характер или предрасположенность.
Используют следующие методы лечения: консервативные, лазерные, хирургические (витреоретинальная хирургия, склеропломбаж при отслойке и др.)
Медикаментозное лечение:
Дезагреганты (Тиклопидин, Клопидогрел, ацетилсалициловая кислота) — принимают внутрь или парентерально; — сосудорасширяющие препараты и ангиопротекторы (Но-шпа, Папаверин, компламин, аскорутин); — антисклеротические средства назначают в основном людям пожилого возраста – метионин, симвастатин, аторвастатин, клофибрат и др.; — комбинированные витаминные препараты (Окувайт-лютеин, Черника-форте и др.), а также внутримышечно витамины группы В; — средства, улучшающие микроциркуляцию (пентоксифиллинпарабульбарно или внутривенно) — полипептиды из сетчатки крупного рогатого скота (Ретиналамин) парабульбарно ежедневно в течение 10 дней. В субтеноново пространство вводят 1 раз в полгода; — биогенные стимуляторы – алоэ, ФИБС, энкад (для лечения тапеторетинальной дистрофии применяют внутримышечно или субконъюнктивально); — местно применяют капли тауфон, эмоксипин по 1 капле 3 раза в день постоянно или на усмотрение врача.
При экссудативной форме возрастной макулодистрофии дексаметазон по 1 мл вводят парабульбарно, а также фуросемид внутривенно капельно. При кровоизлияниях применяют гепарин, этамзилат, аминокапроновую кислоту, проурокиназу. При выраженном отеке в субтеноново пространство вводят триамцинолон. Пути введения, дозировка и длительность лечения зависят от каждого конкретного случая.
Физиотерапия
также эффективна при дистрофиях сетчатки: используют электрофорез с гепарином, но-шпой, никотиновой кислотой и др., магнитотерапию, стимуляцию сетчатки низкоэнергетическим лазерным излучением.
Наиболее эффективным методом лечения считается лазерная коагуляция сетчатки
, при котором отграничивают поврежденные участки от здоровых тканей, тем самым приостанавливая развитие заболевания.
При образовании витреоретинальных сращений и неоваскулярных мембран рекомендована витрэктомия
.
При наследственных дистрофиях сетчатки прогноз неблагоприятный, практически всегда приводят к слепоте.
При возрастной макулодистрофии показано стационарное лечение 2 раза в год, а также рекомендовано ношение солнцезащитных очков и отказ от курения.
Врач офтальмолог Летюк Т.З.
Болезнь Беста — серьезное наследственное офтольмологическое заболевание, которое встречается у 4 человек из 100 тысяч. Главная проблема состоит в том, что недуг протекает бессимптомно на начальных стадиях, и проявляет себя, когда уже зрение стремительно начинает падать.
К счастью, болезнь Беста крайне редко приводит к полной потере зрительной функции. В статье пойдет речь об особенностях заболевания, какие симптомы для него характерны, а также о самых эффективных методах лечения.