Причины
Внутриглазная жидкость или водянистая влага продуцируется цилиарным телом. Она выводится через Шлеммов канал в углу передней камеры глаза.
Причины застоя жидкости:
- изменения угла передней камеры:
- сосудистые новообразования, диабетическая ретинопатия;
- пробки из частиц пигмента, кровяных телец, отделившихся от удара, травмы;
- опухоль.
- катаракта последней стадии;
- увеит;
- иридоциклит.
- повышения ацетилхолина.
Сбой в механизме секреции, циркуляции влаги повышает внутриглазное давление и риск развития глаукомы.
Что это такое?
Водяниста влага — прозрачная жидкость, которая находится в передней и задней камерах глаза. Она продуцируется капиллярами ресничных отростков и дренируется в Шлеммов канал, располагающейся между роговицей и склерой. Внутриглазная влага постоянно циркулирует. Процесс контролируется гипоталамусом. Она находится в периневральных и перивазальных щелях, ретролентальном и перихориоидальнои пространстве.
В журнале «Новое в офтальмологии» опубликованы результаты исследования и доказано главное функционирование увеосклерального пути оттока внутриглазной жидкости среди возможных вариаций.
Классификация глаукомы
По происхождению:
- первичная — развивается после 40 лет, связана с патологическими процессами внутри глазного яблока;
- вторичная — возникает после травм, болезней, операций.
По механизму повышения глазного давления:
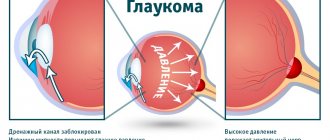
- открытоугольная — «молчаливая», протекает скрыто при свободном движении влаги;
- закрытоугольная — «застойная», канал отхода жидкости заблокирован.
По уровню глазного давления:
- гипертензивная;
- нормотензивная.
По течению болезни:
- стабилизированная — состояние пациента не меняется на протяжении полугода;
- нестабилизированная — ухудшение при повторных исследованиях.
Стадии поражения зрительного нерва:
- начальная — нет заметных изменений поля зрения;
- развитая — сужение в 10° от точки фиксации;
- далеко зашедшая — ограничение поля зрения в 15°;
- терминальная — слепота, иногда сохраняется светоощущение.
Вторичная глаукома протекает с циклитическими кризами.
Камеры глаза. Пути оттока внутриглазной жидкости.
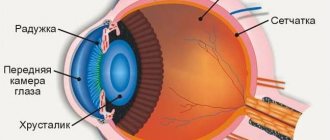
Передняя камера
представляет собой пространство, ограниченное задней поверхностью роговицы, передней поверхностью радужки и центральной частью передней капсулы хрусталика. Место, где роговица переходит в склеру, а радужка в ресничное тело, называется углом передней камеры. Угол передней камеры — наиболее узкая часть передней камеры. Передняя стенка УПК кольцом Швальбе, трабекулярным аппаратом и склеральной шпорой, задняя стенка УПК — корнем радужки, вершина — основанием цилиарной короны. На наружной стенке УПК находится дренажная система глаза.
Дренажная система глаза состоит из трабекулярного аппарата, склерального синуса (шлеммов канал) и коллекторных канальцев. Трабекулярный аппарат представляет собой кольцевидную перекладину, переброшенную через внутреннюю склеральную бороздку. На разрезе он имеет форму треугольника, вершина которого прикрепляется к переднему краю бороздки (пограничное кольцо Швальбе), а основание — к ее заднему краю (склеральная шпора). Трабекулярная диафрагма состоит из трех основных частей: увеальной трабекулы, корнеосклеральной трабекулы и юкстаканаликулярной ткани. Две первые части имеют слоистое строение. Каждый слой (всего их 10-15) представляет собой пластинку, состоящую из коллагеновых фибрилл и эластических волокон, покрытую с обеих сторон базальной мембраной и эндотелием. В пластинах имеются отверстия, а между пластинами — щели, заполненные ВЖ. Юкстаканаликулярный слой, состоящий из 2-3 слоев фиброцитов и рыхлой волокнистой ткани, оказывает наибольшее сопротивление оттоку ВЖ из глаза. Наружная поверхность юкстаканаликулярного слоя покрыта эндотелием, содержащим гигансткие вакуоли. Последние являются динамическими внутриклеточными канальцами, по которым ВЖ переходит из трабекулярного аппарата в шлеммов канал.
Шлеммов канал представляет собой циркулярную щель, выстланную эндотелием и расположенную в задненаружной части внутренней склеральной бороздки. От передней камеры он отделен трабекулярным аппаратом, кнаружи от канала расположена склера и эписклера с венозными и артериальными сосудами. ВЖ оттекает из шлеммова канала по 20-30 коллекторным канальцам в эписклеральные вены (вены-реципиенты).
Через зрачок передняя камера свободно сообщается с задней. Задняя камера
находится за радужкой, которая является ее передней стенкой и ограничена снаружи ресничным телом, сзади стекловидным телом. Внутреннюю стенку образует экватор хрусталика. Все пространство задней камеры пронизано связками ресничного пояска.
В норме обе камеры глаза заполнены водянистой влагой, которая по своему составу напоминает диализат плазмы крови. Водянистая влага содержит питательные вещества (глюкозу, аскорбиновую кислоту, кислород), употребляемые хрусталиком и роговицей, и уносит из глаза продукты обмена (молочную кислоту, углекислый газ, отшелушившиеся пигментные и другие клетки).
Продукция и отток внутриглазной жидкости (ВЖ).
ВЖ непрерывно продуцируется цилиарной короной при активном участии непигментного эпителия сетчатки и в меньшем количестве в процесс ультрафильтрации капиллярной сети. Влага заполняет заднюю камеру, затем через зрачок поступает в переднюю камеру (она служит ее основным резервуаром и имеет вдвое больший объем, чем задняя) и оттекает в основном в эписклеральные вены по дренажной системе глаза, расположенной на передней стенке угла передней камеры. Около 15% жидкости уходит из глаза, просачиваясь через строму цилиарного тела и склеру в увеальные и склеральные вены — увеосклеральный путь оттока ВЖ. Незначительная часть жидкости впитывается радужкой (как губкой) и лимфатической системой.
Регуляция внутриглазного давления . Образование водянистой влаги находится под контролем гипоталамуса. Определенное влияние на секреторные процессы оказывает изменение давления и скорость оттока крови в сосудах ресничного тела. Отток внутриглазной жидкости регулируется при помощи механизма ресничная мышца — склеральная шпора — трабекула. Продольные и радиальные волокна ресничной мышцы передними концами прикрепляются к склеральной шпоре и трабекуле. При ее сокращении шпора и трабекула отходят кзади и кнутри. Натяжение трабекулярного аппарата увеличивается, а отверстия в нем и склеральный синус расширяются.
Передняя камера
(camera anterior) – пространство, спереди ограни–ченное роговицей, сзади радужкой и в области зрачка хрусталиком. Глубина передней камеры вариабельна, она наибольшая в централь–ной части передней камеры, расположенной против зрачка, и достига–ет 3-3,5 мм. В условиях патологии диагностическое значение приоб–ретает как глубина камеры, так и ее неравномерность.
Задняя камера
(camera posterior) расположена позади радужки, которая является ее передней стенкой. Наружной стенкой служит цилиарное тело, задней – передняя поверхность стекловидного тела. Внутреннюю стенку образуют экватор хрусталика и предэкваториальные зоны передней и задней поверхностей хрусталика. Все пространс–тво задней камеры пронизано фибриллами цинновой связки, которые поддерживают хрусталик в подвешенном состоянии и соединяют его с ресничным телом. Камеры глаза заполнены водянистой влагой – прозрачной бес–цветной жидкостью плотностью 1,005-1,007 с показателем прелом–ления 1,33. Количество влаги у человека не превышает 0,2-0,5 мл. Вырабатываемая отростками цилиарного тела водянистая влага содержит соли, аскорбиновую кислоту, микроэлементы.
Дренажная система
Дренажная система – это основной путь оттока внутриглазной жидкости. Внутриглазная жидкость вырабатывается отростками цилиарного тела. Каждый отросток состоит из стромы, широких тонкостенных капилляров и двух слоев эпителия. Эпителиальные клетки отделены от стромы и от задней камеры наружной и внутренней пограничными мембранами. Поверхности клеток, обращенные к мембранам, имеют хорошо развитые оболочки с многочисленными складками и вдавлениями, как у секреторных клеток. Рассмотрим пути оттока внутриглазной жидкости из глаза (гидро–динамику глаза). Переход внутриглазной жидкости из задней камеры, куда она сначала поступает, в переднюю, в норме не встречает сопро–тивления. Особую важность представляет отток влаги через дренажную систему глаза, расположенную в углу передней камеры (место, где роговица пере–ходит в склеру, а радужка – в ресничное тело) и состоящую из трабекулярного аппарата, шлеммова канала, коллекторных каналов, системы интра– и эписклеральных венозных сосудов. Трабекула имеет сложное строение и состоит из увеальной трабекулы, корнеосклеральной трабекулы и юкстаканаликулярного слоя. Первые две части состоят из 10-15 слоев, образованных пластинами из коллагеновых волокон, покрытых с обеих сторон базальной мем–браной и эндотелием, которые можно рассматривать как многоярус–ную систему щелей и отверстий. Самый наружный, юкстаканаликулярный слой значительно отличается от других. Он представляет собой тонкую диафрагму из эпителиальных клеток и рыхлой системы коллагеновых волокон, пропитанных мукополисахаридами. Та часть сопротивления оттоку внутриглазной жидкости, которая приходится на трабекулу, находится именно в этом слое. Далее идет шлеммов канал или склеральный синус, который впер–вые обнаружил в бычьем глазу в 1778 г. Фонтан, а в 1830 г. подробно описал Шлемм у человека. Шлеммов канал представляет собой циркулярную щель, рас–положенную в зоне лимба. На наружной стенке шлеммова канала расположены выходные отверстия коллекторных каналов (20-35), впервые описанные в 1942 г. Ашером. На поверхности склеры они носят название водяных вен, которые впадают в интра– и эписклеральные вены глаза. Функция трабекулы и шлеммова канала состоит в поддержании постоянства внутриглазного давления. Нарушение оттока внутриглазной жидкости через трабекулу является одной из основных причин первичной глаукомы.
По эписклеральной и интрасклеральной венозной сетке переднего сегментированного участка глазного яблока циркулирует водянистая влага. Она поддерживает процессы обмена веществ , трабекулярного аппарата. При нормальных обстоятельствах глаз человека включает 300 мм компонента или 4% от общего объема.
Жидкость производится из крови особенными клетками, входящими в структуру цилиарного тела. Глаз человека вырабатывает 3-9 мл компонента в минуту. Отток влаги происходит посредством эписклеральных сосудов, увеосклеральной системы и трабекулярной сети. Внутриглазное давление – есть отношение выработанного компонента к выведенному.
Симптомы
Скопление жидкости внутри глаза не ощущается. Признаки состояния:
- сокращение бокового зрения;
- ореолы вокруг объектов;
- нечеткие края изображения.
Симптомы криза:
- острая боль с резким повышением ВГД;
- зрение падает до светоощущения;
- гиперемия;
- тошнота;
- головная боль;
- боль, отдающая под лопатку, в сердце, живот.
Приступ необходимо снять в течение суток. Иначе спайки в тканях глаза еще больше затруднят отток жидкости.
Увеосклеральный отток и его роль в регуляции офтальмотонуса
Т.В. Ставицкая Кафедра глазных болезней Российского государственного медицинского университета, Москва
Более 30 лет назад A. Bill впервые описал возможность фильтрации внутриглазной жидкости не только по дренажной системе глаза, но и через передний отдел сосудистого тракта. Используя меченный альбумин, A.Bill выявил, что у обезьян около 50% жидкости оттекает через передний отдел ресничного тела вдоль волокон цилиарной мышцы в супрахориоидальное пространство. Далее жидкость оттекает по эмиссариям и прямо через склеру [7]. Кроме того, водянистая влага, возможно, всасывается в венозные отделы капилляров сосудистой оболочки [2]. Схема оттока внутриглазной жидкости через передний отдел сосудистого тракта представлена на рис. 1.
Дальнейшие исследования подтвердили полученные A. Bill результаты. В настоящий момент известно, что у обезьян по увеосклеральной системе оттекает около 40–60% внутриглазной жидкости, у кроликов и кошек – только 3–8%, у собак – около 18% [1].
Было выявлено наличие увеосклерального оттока и у людей. Морфологические исследования показали сходство строения и изменения с возрастом цилиарной мышцы и супрахориоидального пространства у высших приматов и человека. Морфологическое изучение изменений цилиарной мышцы с возрастом выявило, что у пожилых людей наблюдается уплотнение экстрацеллюлярного матрикса, которое увеличивается с возрастом. Сравнение строения цилиарной мышцы у больных первичной открытоугольной глаукомой (ПОУГ) и здоровых лиц того же возраста показало, что у больных ПОУГ наблюдается так называемые SD-plaque изменения в передних отделах ресничной мышцы. Изменение строения цилиарной мышцы с возрастом сопровождается снижением оттока жидкости по увеосклеральной системе. Так, у молодых людей он составляет около 36%, а после 60 лет – только 4–14% [1].
Также на состояние увеосклерального оттока влияет степень напряжения ресничной мышцы. При напряжении аккомодации и сокращении цилиарной мышцы сдавливаются свободные пространства экстрацеллюлярного матрикса и отток жидкости снижается, а при расслаблении цилиарной мышцы отток увеличивается [2].
По данным A. Bill и C. Philips, циклоплегические препараты увеличивают увеосклеральный отток (на фоне применения атропина увеосклеральный отток составляет 4–27%), а пилокарпин снижает его (на фоне применения пилокарпина он был равен 0–3%) [1].
Исследования А.П. Нестерова и И.Н. Черкасовой показали, что увеосклеральный отток функционирует только тогда, когда давление в передней камере превышает давление в супрахориоидальном пространстве не менее чем на 2 мм рт. ст. [2].
Таким образом, повышение офтальмотонуса не сопровождается усилением увеосклерального оттока, так как при увеличении внутриглазного давления (ВГД) повышается давление в супрахориоидальном пространстве и оно суживается [2].
Исследования влияния различных веществ на состояние увеосклерального оттока выявили, что местное введение некоторых простагландинов сопровождается снижением офтальмотонуса вследствие усиления увеосклерального оттока водянистой влаги [3]. Согласно последним данным, усиление увеосклерального оттока обусловлено изменением экстрацеллюлярного матрикса (ЭЦМ) ресничной мышцы. Применение простагландинов Fa2 увеличивает содержание матричных металлопротеиназ (ММП) в тканях ресничной мышцы. ММП представляют собой семейство энзимов, обладающих специфичностью по отношению к таким компонентам ЭЦМ, как коллаген, фибронектин и другие. ММП секретируются как неактивные проэнзимы и экстрацеллюлярно превращаются в активные ферменты, которые могут разлагать фибриллы коллагена, в результате чего происходит разрежение ЭЦМ [1].
Действие естественных простагландинов и их аналогов обусловлено агонизмом по отношению к различным простаноидным рецепторам. Существует пять главных рецепторов к простаноидам: DP, EP, FP, IP и TP. Простаноидные рецепторы EP подразделяются на 4 подтипа (EP1, EP2, EP3, EP4). В гладкомышечной ткани выявлены рецепторы типа FP, EP1, EP2, EP3. Естественные простагландины и их аналоги селективны по отношению к различным подтипам рецепторов [4].
Одним из аналогов естественных простагландинов является латанопрост – синтетический фенилзамещенный аналог простагландина Fa2. Латанопрост проявляет высокую селективность по отношению к рецепторам FP, что обусловливает его высокую терапевтическую эффективность.
Латанопрост выпускается в виде 0,005% раствора во флаконах по 2,5 мл. Предварительные исследования выраженности гипотензивного эффекта при использовании различных концентраций раствора латанопроста показали, что наибольшей терапевтической эффективностью обладает раствор латанопроста, содержащий 50 мкг/мл и применяемый 1 раз в день (на ночь) [1]. Изменения ВГД на фоне применения различных доз латанопроста показаны на рис. 2.
Гипотензивное действие латанопроста обусловлено улучшением увеосклерального пути оттока. Степень изменения увеосклерального пути оттока на фоне применения латанопроста отражена на рис. 3.
Сравнительные исследования эффективности 0,5% раствора тимолола малеата, применяемого 2 раза в день, и 0,005% раствора латанопроста, используемого 1 раз в день, показали, что латанопрост у большего числа больных и в большей степени снижает офтальмотонус. По данным A. Alm, у 56% больных, получавших латанопрост, ВГД было ниже или равно 17 мм рт.ст., а у 27% пациентов оно было ниже 15 мм рт.ст. В группе тимолола малеата только у 38% больных офтальмотонус был ниже 17 мм рт.ст. и у 14% – ниже 15 мм рт.ст. [3].
Анализ трех рандомизированных двойных слепых клинических исследований показал, что снижение офтальмотонуса на фоне применения латанопроста в течение 6 мес составило 8,0±0,1 мм рт.ст., в то время, как в группе тимолола ВГД уменьшилось на 6,7±0,1 мм рт.ст. Разница между двумя методами лечения составила 1,3 мм рт.ст. [5].
По данным C. Hartleben, гипотензивное действие латонопроста более выражено по сравнению с 2% раствором дорзоламида гидрохлорида, применяемого 3 раза в день. По его данным, офтальмотонус был ниже 18 мм рт.ст. у 46% больных, получавших латанопрост, и только у 9% пациентов, использовавших дорзоламид [6].
Результаты исследований, проведенных J. Nordmann и B. Kovacs, выявили более высокую эффективность латанопроста по сравнению с комбинацией тимолола и пилокарпина. Офтальмотонус снизился на фоне применения латанопроста в среднем на 5,4±0,3 мм рт.ст., в то время как в группе больных, получавших комбинацию тимолола и пилокарпина, снижение ВГД составило 4,9±0,4 мм рт.ст. [7, 8].
По данным J. Sanchez, монотерапия латанопростом оказалась более эффективной по сравнению с комбинированным применением тимолола и дорзоламида. Через 3 мес лечения латанопростом ВГД уменьшилось на 5,2 мм рт.ст., что составило 23% от исходного уровня. А в группе больных, получавших комбинацию тимолола и дорзоламида, уменьшение офтальмотонуса составило 4 мм рт.ст. или 17% от исходного уровня [9, 10].
В выборе медикаментозной терапии глаукомы огромное значение имеет возможность длительного применения препарата без снижения выраженности его гипотензивного действия. Исследования, проведенные в Великобритании, показали, что в среднем у 93% больных поддерживается среднее снижение ВГД на 32% по отношению к исходному уровню на фоне 2-летнего применения латанопроста [11].
Довольно часто монотерапия лекарственными средствами не сопровождается достаточной компенсацией ВГД. Поэтому требуется сочетанное применение гипотензивных препаратов. Ряд исследований, проведенных как в нашей стране, так и за рубежом, позволили выявить наиболее эффективные комбинации латанопроста и других глазных капель. Так, по данным Е.А. Егорова и О.В. Романовой, наиболее целесообразно совместное применение латанопроста с тимололом, дипивефрином, эпинефрином и апроклонидином [12]. Полученные ими данные подтверждаются исследованиями ряда зарубежных авторов.
Таким образом, стимуляция увеосклерального оттока сопровождается выраженным снижением офтальмотонуса. Однако применение препаратов, которые облегчают отток жидкости по увеосклеральной системе сопровождается рядом побочных эффектов. У некоторых больных при длительном применении (более 3 мес) наблюдается усиление пигментации радужки и удлинение ресниц. Пигментация появляется преимущественно у больных с неравномерной окраской радужки. Монохромные (зелено-карие) радужки практически не подвергаются гиперпигментации. Имеются единичные сообщения о возможном развитии отека в центральной зоне сетчатки на фоне применения латанопроста и усиление воспалительной реакции сосудистой оболочки.
В заключение следует остановиться на ряде исследований зависимости стоимости лечения глаукомы от выбора терапии. G. Kobelt и соавт. отмечают, что исходное значение офтальмотонуса положительно коррелирует со стоимостью лечения (т.е. чем выше исходное ВГД, тем более интенсивным было лечение и, следовательно, тем выше была его стоимость), в то время как снижение ВГД после начала терапии отрицательно коррелировало со стоимостью (чем лучше первоначально уменьшался офтальмотонус, тем меньше была последующая стоимость лечения). Моделирование эффекта применения новых видов препаратов на стоимость терапии показало, что назначение эффективной медикаментозной терапии и потенциальное уменьшение частоты использования хирургических методов лечения могут частично компенсировать дополнительную стоимость новых препаратов [13].
Литература
1. A. Alm et al. Uveoscleral outflow.//Mosby-Wolfe,1998.
2. А.П. Нестеров. Глаукома.// М. Медицина, 1995.
3. A. Alm. Target IOP-definitions and strategies to reach it.// Report from the symposium: targeting the Uveoscleral outflow-the New Approach to IOP Reduction. Stockholm, June 27-July 1,1999; p.16.
4. Б. Ресул. Рецепторный профиль аналогов простагландина F: латанопроста и изопропил-унопростона, используемых в качестве глазных гипотензивных препаратов.// Сборник материалов 2-го Международного симпозиума по глаукоме. Иерусалим, Израиль, 15–20 марта 1998 г.
5. Hedman K. et al. Мета анализ трех рандомизированных, двойных слепых клинических исследований III фазы, сравнивающих латанопрост с тимололом у больных открытоугольной глаукомой и офтальмогипертензией.// Ophthalmological abstract journal, 1999; 18 (1).
6. C. Hartleben. Comparison of latanoprost 0,005% once daily with timolol 0,5% twise daily in Hispanic patients with open-angle glaucoma or ocular hypertension.// Report from the symposium: targeting the Uveoscleral outflow-the New Approach to IOP Reduction. Stockholm, June 27-July 1, 1999; p. 28.
7. B.Kovacs. A switch to latanoprost monotherapy as an alternative to adding pilocarpaine to timolol in patients inadequately controlled on a topical beta-blocker.// Report from the symposium: targeting the Uveoscleral outflow-the New Approach to IOP Reduction. Stockholm, June 27-July 1,1999; р. 34.
8. J.P. Nordmann. Comparison of the intraocular pressure-lowering effect of latanoprost and a fixed combination of timolol-pilocarpine in patients insufficiently controlled with beta-adrenergic antagonists.// Report from the symposium: targeting the Uveoscleral outflow-the New Approach to IOP Reduction. Stockholm, June 27-July 1,1999; p. 33.
9. E.O’Donoghue. Comparison of latanoprost and dorsolamide in patients with glaucoma and ocular hypertension.// Report from the symposium: targeting the Uveoscleral outflow-the New Approach to IOP Reduction. Stockholm, June 27-July 1, 1999; p.29.
10. J.G. Sanchez A 3-month comparison of latanoprost monotherapy to dorzolamide as adjunctive therapy to timolol in patients inadequately controlled on a topical beta-blocker. // Report from the symposium: targeting the Uveoscleral outflow-the New Approach to IOP Reduction. Stockholm, June 27-July 1, 1999; p. 38.
11. Hedman K. Влияние латанопроста на внутриглазное давление в течение 24-месячного периода лечения.// Ophthalmological abstract journal, 1999; 1: 18 (1).
12. Егоров Е.А., Романова О.В. Перспективы применения аналога простагландина Fa2 – латанопроста в гипотензивной терапии глаукомы.// Вестн. офтальмол.,1998; 4: 19–20.
13. Kobelt G. et al. Стоимость лечения первичной открытоугольной глаукомы и офтальмогипертензии. Ретроспективный обзор историй болезни при двухлетнем наблюдении у больных с впервые установленным диагнозом в Швеции и США.// Ophthalmological abstract journal, 1999; 18 (1).
Приложения к статье
Стимуляция увеосклерального оттока сопровождается выраженным снижением офтальмотонуса
Рис. 1. Схема увеосклерального оттока внутриглазной жидкости
Рис. 2. Изменение ВГД на фоне применения различных доз латанопроста. (По данным А. Alm. Prostaglandin Fa2-isopropylester eye drops: effects in normal human eyes.// Br. J. Ophthalmol. 1989; 73: 419-26)
Рис. 3. Изменение увеосклерального оттока на фоне применения латанопроста
(Visited 14 times, 1 visits today)
Лечение
На начальной стадии процесса назначают глазные капли:
- стимулирующие отток жидкости
- подавляют ее выработку.
Также их комбинируют.
Приступ снимают каплями Пилокарпин, Тимолол, Бетаксолол. Если через 20 часов ВГД не снижается, делают операцию:
- трабекулоэктомия — хирургическое формирование дренажного канала;
- иридэктомия — частичное иссечение радужной оболочки;
- оптико-цилиарная нейроэктомия — удаление части ресничного, зрительного нерва.
Оперативное лечение также назначают при неэффективности консервативного метода.
Профилактика
Как предотвратить повторное развитие глаукомы:
- проходить осмотр раз в 3 месяца;
- избегать темноты;
- при работе за компьютером, просмотре телевизора включать лампу;
- смотреть телевизор не более 3 часов в день;
- отказаться от алкоголя, курения;
- надевать защитные очки с зелеными стеклами;
- ежедневно выполнять массаж глаз;
- отказаться от тяжелых физических нагрузок.
Диета должна включать рыбу, овощи, но следует ограничить содержание сахара, отказаться от кофе.